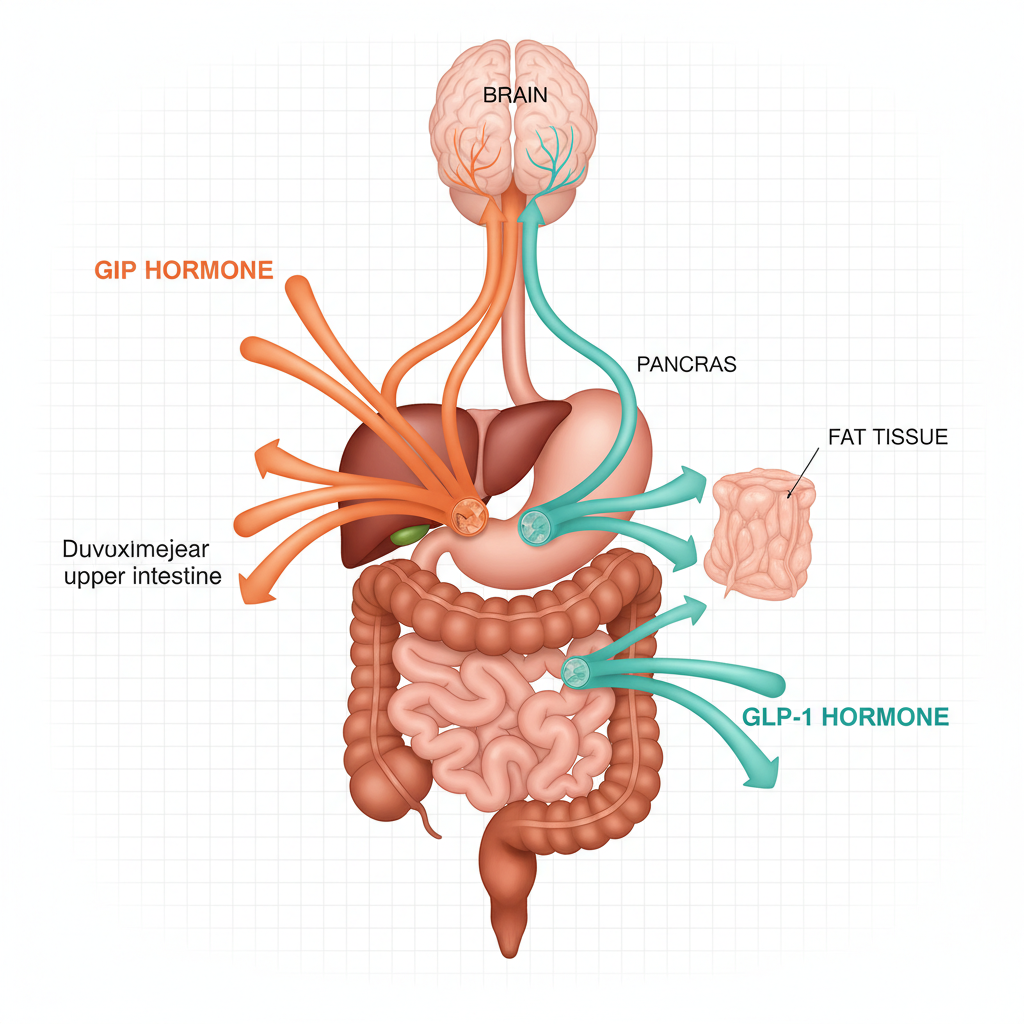
Las hormonas incretinas GLP-1 y GIP desempeñan un papel central en la regulación del apetito, el metabolismo de la glucosa y el peso corporal. Comprender su funcionamiento permite entender mejor por qué el tirzepatide (Mounjaro), que se dirige a estas dos hormonas simultáneamente, obtiene resultados superiores a los tratamientos monoagonistas.
Incretinas: hormonas digestivas esenciales
El concepto de incretina surgió de una observación clínica importante: la administración oral de glucosa provoca una secreción de insulina significativamente superior a la obtenida por inyección intravenosa de la misma cantidad de glucosa. Este efecto incretina, descubierto en la década de 1960, representa entre el 50 y el 70% de la respuesta insulínica posprandial total.
Dos hormonas son responsables de este efecto: el GLP-1 (péptido-1 similar al glucagón) y el GIP (polipéptido insulinotrópico dependiente de glucosa). Secretadas por células especializadas del intestino en respuesta a la ingesta de alimentos, orquestan una cascada de señales metabólicas que van mucho más allá de la simple regulación de la glucemia.
GLP-1: la hormona de la saciedad
El GLP-1 es sintetizado por las células L del íleon distal y del colon a partir del proglucagón, un precursor peptídico. Su secreción comienza entre 10 y 15 minutos después del inicio de una comida, con un pico alcanzado entre 30 y 60 minutos.
Mecanismos de acción del GLP-1:
En el páncreas: El GLP-1 se une a su receptor (GLP-1R) en las células beta pancreáticas, estimulando la secreción de insulina de manera glucosa-dependiente. Esto significa que el efecto insulinosecretor solo se manifiesta cuando la glucemia es elevada, lo que minimiza el riesgo de hipoglucemia. También inhibe la secreción de glucagón por las células alfa, reduciendo la producción hepática de glucosa.
En el cerebro: Los receptores de GLP-1 están presentes en varias regiones cerebrales implicadas en el control del apetito: el núcleo del tracto solitario (NTS) en el tronco encefálico, el núcleo arqueado del hipotálamo y el área postrema. La activación de estos receptores reduce las señales de hambre y aumenta la sensación de saciedad. El GLP-1 también modula el sistema de recompensa dopaminérgico, disminuyendo el atractivo por los alimentos ricos en grasas y azúcares (Turton et al., Nature, 1996).
En el estómago: El GLP-1 ralentiza significativamente el vaciamiento gástrico, lo que prolonga la distensión del estómago y las señales mecánicas de saciedad. Este efecto explica en parte las náuseas observadas al inicio del tratamiento con agonistas de GLP-1.
En el sistema cardiovascular: Los receptores de GLP-1 se expresan en los cardiomiocitos y las células endoteliales. El GLP-1 mejora la función endotelial, reduce la inflamación vascular y ha demostrado efectos cardioprotectores en grandes estudios cardiovasculares (LEADER, SUSTAIN-6, SELECT).
Vida media natural del GLP-1: solo 2 a 3 minutos. La enzima DPP-4 (dipeptidil peptidasa-4) degrada rápidamente el GLP-1 en metabolitos inactivos. Esta degradación ultrarrápida hizo necesaria el desarrollo de formas resistentes (análogos de GLP-1) o de inhibidores de la DPP-4.
GIP: la hormona metabólica poco conocida
El GIP es secretado por las células K del duodeno y el yeyuno proximal. Su secreción se desencadena principalmente por la absorción de glucosa y lípidos, con un pico plasmático alcanzado entre 15 y 30 minutos después de la comida.
Considerado durante mucho tiempo una hormona menor en la fisiología metabólica, el GIP ha sido objeto de una reevaluación completa desde los trabajos de Muller et al. (Nature Reviews Drug Discovery, 2022).
Mecanismos de acción del GIP:
En el páncreas: El GIP es el estimulador más potente de la secreción de insulina entre las incretinas, responsable de aproximadamente el 60% del efecto incretina total. Al igual que el GLP-1, su acción es glucosa-dependiente. También estimula la proliferación y supervivencia de las células beta pancreáticas.
En el tejido adiposo: Aquí es donde el GIP se distingue fundamentalmente del GLP-1. Los receptores de GIP (GIP-R) se expresan fuertemente en el tejido adiposo blanco. La activación del GIP-R en el tejido adiposo produce efectos complejos y dependientes del contexto:
- En condiciones fisiológicas normales: el GIP favorece el almacenamiento de lípidos y la adipogénesis
- En activación farmacológica sostenida (como con el tirzepatide): favorece la lipólisis, la movilización de grasas y el pardeamiento del tejido adiposo blanco
- Mejora la sensibilidad a la insulina en el tejido adiposo
- Reduce la inflamación adipocitaria crónica asociada a la obesidad
En el cerebro: Los receptores de GIP están presentes en el hipotálamo, la corteza cerebral y el hipocampo. El GIP modula el apetito a través de vías distintas a las del GLP-1, actuando notablemente sobre la motivación alimentaria y los circuitos de recompensa. Estudios en ratones muestran que la activación de las neuronas GIP-R en el hipotálamo reduce la ingesta de alimentos de manera independiente del GLP-1 (Kaneko et al., Cell Metabolism, 2023).
En los huesos: El GIP estimula la formación ósea activando los osteoblastos e inhibiendo parcialmente la resorción ósea. Por ello, el tirzepatide podría tener una ventaja sobre los agonistas puros de GLP-1 para la preservación de la densidad ósea durante la pérdida de peso.
Vida media natural del GIP: aproximadamente 5 a 7 minutos, también degradado por la DPP-4.
La diferencia entre pacientes sanos y diabéticos
Una paradoja frenó durante mucho tiempo el desarrollo de terapias basadas en el GIP: en pacientes con diabetes tipo 2, la respuesta insulínica al GIP está gravemente alterada. El efecto incretina se reduce en un 80% en comparación con sujetos sanos.
| Parámetro | Sujeto sano | Diabetes tipo 2 |
|---|---|---|
| Efecto incretina total | 50-70 % | 20-30 % |
| Respuesta al GIP | Normal | Gravemente reducida |
| Respuesta al GLP-1 | Normal | Parcialmente preservada |
| Secreción de GLP-1 | Normal | Ligeramente reducida |
| Secreción de GIP | Normal | Normal o aumentada |
Fuente: Nauck MA, Meier JJ. Diabetologia. 2011;54(1):10-18.
Esta paradoja se resolvió con el descubrimiento de que la activación farmacológica suprafisiológica del receptor de GIP (como la producida por el tirzepatide) puede restaurar la sensibilidad al GIP en pacientes diabéticos, superando incluso la respuesta fisiológica normal.
Sinergia GLP-1 + GIP: por qué 1 + 1 = 3
La asociación de las dos hormonas produce efectos sinérgicos que superan la simple suma de sus acciones individuales:
1. Sobre la pérdida de peso: El GLP-1 reduce el apetito a través del tronco encefálico y ralentiza el vaciamiento gástrico. El GIP activa vías complementarias en el hipotálamo y actúa directamente sobre el tejido adiposo. Resultado: la pérdida de peso con tirzepatide (22,5%) es de 5 a 6 puntos porcentuales superior a la obtenida con semaglutide (16,9%).
2. Sobre el control glucémico: La doble estimulación insulinosecretora potencia la respuesta pancreática. La reducción de la HbA1c es del 2,07% con tirzepatide 15 mg, frente al 1,86% con semaglutide 2 mg.
3. Sobre la composición corporal: El GIP favorece la pérdida de masa grasa mientras preserva la masa magra. El estudio SURMOUNT-1 mostró que el 85% de la pérdida de peso con tirzepatide provino de la masa grasa, una proporción superior a la observada con semaglutide.
4. Sobre la tolerabilidad: El sesgo de señalización del tirzepatide en el receptor de GLP-1 (favoreciendo la vía de AMPc frente a la beta-arrestina) reduce los efectos gastrointestinales. Las náuseas son generalmente menos graves y de menor duración que con semaglutide.
Aplicaciones terapéuticas actuales y futuras
La comprensión de la fisiología de las incretinas ha permitido el desarrollo de cuatro clases de medicamentos:
- Inhibidores de la DPP-4 (sitagliptina, vildagliptina): impiden la degradación de las incretinas naturales. Efectos modestos sobre el peso y la glucemia.
- Agonistas del receptor de GLP-1 (semaglutide, liraglutide, dulaglutide): imitan la acción del GLP-1 con una duración de acción prolongada.
- Doble agonista GIP/GLP-1 (tirzepatide): primera molécula en activar ambos receptores simultáneamente.
- Triple agonista GIP/GLP-1/glucagón (retatrutide, en fase 3): añade el receptor de glucagón para aumentar aún más el gasto energético.
Puntos clave
El GLP-1 y el GIP son dos hormonas complementarias que, juntas, controlan más de la mitad de la respuesta insulínica después de una comida. Mientras que el GLP-1 actúa principalmente sobre el apetito, el vaciamiento gástrico y el sistema cardiovascular, el GIP desempeña un papel único en el metabolismo del tejido adiposo y la formación ósea. El tirzepatide aprovecha esta complementariedad para producir resultados clínicos superiores a los tratamientos que se dirigen a una sola hormona.
Preguntas Frecuentes
¿Cuál es la diferencia entre GLP-1 y GIP?
El GLP-1 actúa principalmente sobre el apetito (a través del cerebro), el vaciamiento gástrico y el páncreas. El GIP se dirige más al tejido adiposo, el metabolismo óseo y la respuesta insulínica pancreática. Ambas son hormonas incretinas secretadas por el intestino después de una comida.
¿Por qué el GIP fue ignorado durante tanto tiempo en los tratamientos?
En pacientes diabéticos, la respuesta natural al GIP está muy alterada. Los investigadores pensaban, por lo tanto, que dirigirse al GIP sería ineficaz. El tirzepatide demostró lo contrario: la activación farmacológica a dosis suprafisiológicas restaura y amplifica los efectos del GIP.
¿El GLP-1 natural dura mucho tiempo en el cuerpo?
No. El GLP-1 natural tiene una vida media de solo 2 a 3 minutos antes de ser degradado por la enzima DPP-4. Por eso, los medicamentos agonistas de GLP-1 se modifican químicamente para resistir esta degradación y durar varios días.
¿El tirzepatide estimula ambas hormonas o las reemplaza?
El tirzepatide no estimula la secreción natural de GLP-1 y GIP. Reemplaza su acción activando directamente sus receptores celulares, como una llave que abriría dos cerraduras diferentes simultáneamente.
¿Son los inhibidores de la DPP-4 tan efectivos como los agonistas?
No. Los inhibidores de la DPP-4 (como la sitagliptina) impiden la degradación de las incretinas naturales, pero solo aumentan sus niveles de 2 a 3 veces. Los agonistas como el tirzepatide alcanzan concentraciones de 10 a 100 veces superiores a los niveles fisiológicos, produciendo efectos mucho más potentes sobre el peso y la glucemia.
Fuentes
- Nauck MA, Meier JJ. The incretin effect in healthy individuals and those with type 2 diabetes. Diabetologia. 2011;54(1):10-18.
- Muller TD et al. GIP and GLP-1 as therapeutic targets in diabetes and obesity. Nat Rev Drug Discov. 2022;21:513-532.
- Turton MD et al. A rôle for glucagon-like peptide-1 in the central régulation of feeding. Nature. 1996;379:69-72.
- Kaneko K et al. GIP receptor signaling in neurons mediates body weight réduction. Cell Metabolism. 2023.
- Campbell JE, Drucker DJ. Pharmacology, physiology, and mechanisms of incretin hormone action. Cell Metab. 2013;17(6):819-837.
- Holst JJ. The physiology of glucagon-like peptide 1. Physiol Rev. 2007;87(4):1409-1439.