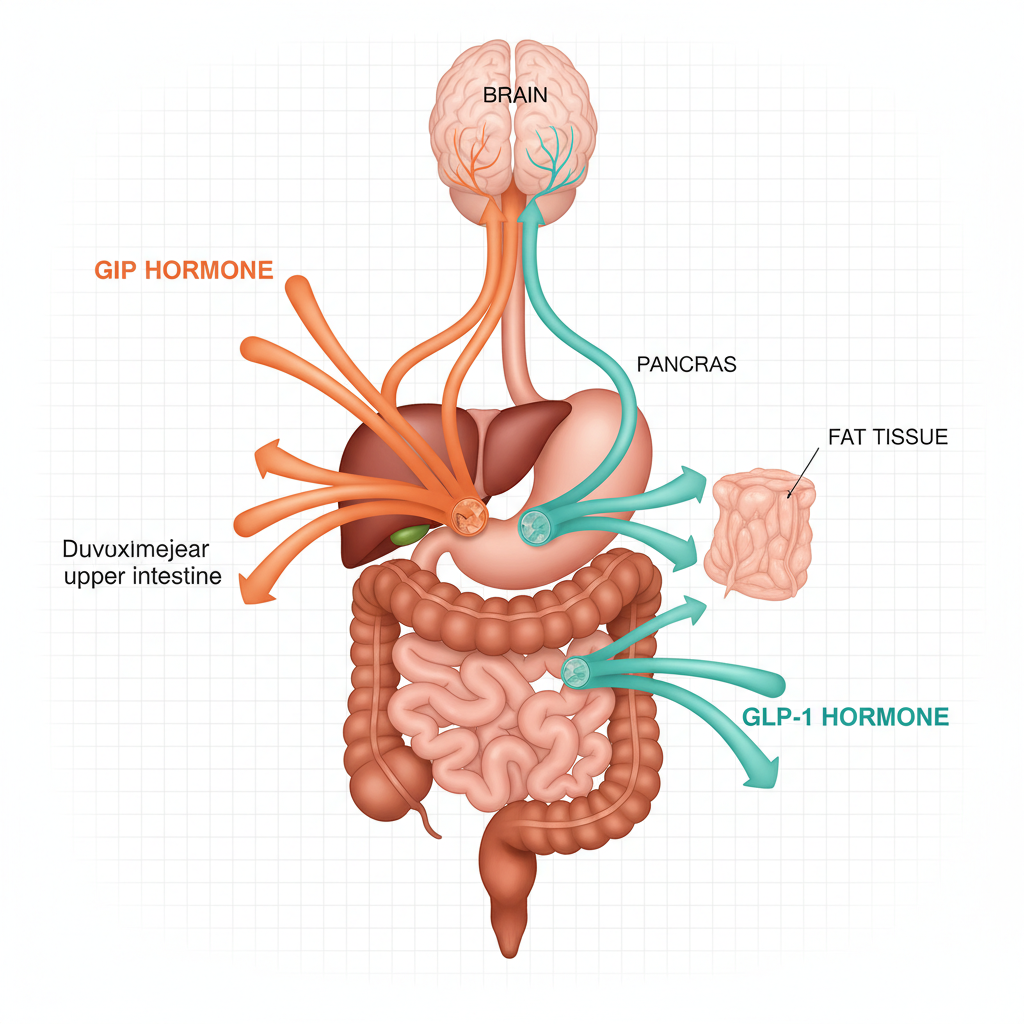
Les hormones incrétines GLP-1 et GIP jouent un rôle central dans la régulation de l’appétit, du métabolisme glucidique et du poids corporel. Comprendre leur fonctionnement permet de mieux apprehender pourquoi le tirzépatide (Mounjaro), qui cible ces deux hormones simultanement, obtient des résultats supérieurs aux traitements mono-agonistes.
Les incrétines : des hormones digestives essentielles
Le concept d’incrétine est ne d’une observation clinique majeure : l’administration orale de glucose provoque une sécrétion d’insuline nettement supérieure a celle obtenue par injection intraveineuse de la même quantité de glucose. Cet effet incrétine, decouvert dans les annees 1960, représente 50 a 70 % de la réponse insulinique post-prandiale totale.
Deux hormones sont responsables de cet effet : le GLP-1 (glucagon-like peptide-1) et le GIP (glucose-dépendent insulinotropic polypeptide). Secretees par des cellules specialisees de l’intestin en réponse a l’ingestion d’aliments, elles orchestrent une cascade de signaux métaboliques qui depassent largement la simple régulation de la glycémie.
Le GLP-1 : l’hormone de la satiété
Le GLP-1 est synthetise par les cellules L de l’ileon distal et du côlon à partir du proglucagon, un precurseur peptidique. Sa sécrétion debute 10 a 15 minutes après le début d’un repas, avec un pic atteint entre 30 et 60 minutes.
Mecanismes d’action du GLP-1 :
Sur le pancreas : Le GLP-1 se lie a son récepteur (GLP-1R) sur les cellules beta pancreatiques, stimulant la sécrétion d’insuline de manière glucose-dependante. Cela signifie que l’effet insulino-secreteur ne se manifeste que lorsque la glycémie est élevée, ce qui minimise le risque d’hypoglycémie. Il inhibe egalement la sécrétion de glucagon par les cellules alpha, reduisant la production hépatique de glucose.
Sur le cerveau : Les récepteurs GLP-1 sont présents dans plusieurs régions cérébrales impliquees dans le contrôle de l’appétit : le noyau du tractus solitaire (NTS) dans le tronc cerebral, le noyau arque de l’hypothalamus, et l’area postrema. L’activation de ces récepteurs réduit les signaux de faim et augmente la sensation de satiété. Le GLP-1 module egalement le système de recompense dopaminergique, diminuant l’attrait pour les aliments riches en graisses et en sucres (Turton et al., Nature, 1996).
Sur l’estomac : Le GLP-1 ralentit significativement la vidange gastrique, ce qui prolonge la distension de l’estomac et les signaux mecaniques de satiété. Cet effet explique en partie les nausées observees en début de traitement par agonistes GLP-1.
Sur le système cardiovasculaire : Des récepteurs GLP-1 sont exprimes sur les cardiomyocytes et les cellules endotheliales. Le GLP-1 amélioré la fonction endotheliale, réduit l’inflammation vasculaire et à des effets cardioprotecteurs demontres dans les grandes études cardiovasculaires (LEADER, SUSTAIN-6, SELECT).
Demi-vie naturelle du GLP-1 : seulement 2 a 3 minutes. L’enzyme DPP-4 (dipeptidyl peptidase-4) degrade rapidement le GLP-1 en metabolites inactifs. C’est cette degradation ultrarapide qui a nécessité le développement de formes resistantes (analogues GLP-1) ou d’inhibiteurs de la DPP-4.
Le GIP : l’hormone métabolique meconnue
Le GIP est secrete par les cellules K du duodenum et du jejunum proximal. Sa sécrétion est declenchee principalement par l’absorption de glucose et de lipides, avec un pic plasmatique atteint 15 a 30 minutes après le repas.
Longtemps considere comme une hormone mineure dans la physiologie métabolique, le GIP fait l’objet d’une reevaluation complète depuis les travaux de Muller et al. (Nature Reviews Drug Discovery, 2022).
Mecanismes d’action du GIP :
Sur le pancreas : Le GIP est le plus puissant stimulateur de la sécrétion d’insuline parmi les incrétines, responsable d’environ 60 % de l’effet incrétine total. Comme le GLP-1, son action est glucose-dependante. Il stimule egalement la proliferation et la survie des cellules beta pancreatiques.
Sur le tissu adipeux : C’est ici que le GIP se distingue fondamentalement du GLP-1. Les récepteurs du GIP (GIP-R) sont fortement exprimes dans le tissu adipeux blanc. L’activation du GIP-R dans le tissu adipeux produit des effets complexes et dependants du contexte :
- En conditions physiologiques normales : le GIP favorise le stockage des lipides et l’adipogenese
- En activation pharmacologique soutenue (comme avec le tirzépatide) : il favorise la lipolyse, la mobilisation des graisses et le brunissement du tissu adipeux blanc
- Il amélioré la sensibilite a l’insuline dans le tissu adipeux
- Il réduit l’inflammation adipocytaire chronique associee a l’obésité
Sur le cerveau : Des récepteurs GIP sont présents dans l’hypothalamus, le cortex cerebral et l’hippocampe. Le GIP module l’appétit par des voies distinctes de celles du GLP-1, agissant notamment sur la motivation alimentaire et les circuits de recompense. Des études chez la souris montrent que l’activation des neurones GIP-R dans l’hypothalamus réduit la prise alimentaire de manière independante du GLP-1 (Kaneko et al., Cell Metabolism, 2023).
Sur les os : Le GIP stimule la formation osseuse en activant les osteoblastes et en inhibant partiellement la resorption osseuse. C’est pourquoi le tirzépatide pourrait avoir un avantage sur les agonistes purs du GLP-1 pour la preservation de la densite osseuse pendant la perte de poids.
Demi-vie naturelle du GIP : environ 5 a 7 minutes, egalement degrade par la DPP-4.
La différence entre patients sains et diabétiques
Un paradoxe a longtemps freine le développement de thérapies basees sur le GIP : chez les patients diabétiques de type 2, la réponse insulinique au GIP est severement alteree. L’effet incrétine est réduit de 80 % par rapport aux sujets sains.
| Parametre | Sujet sain | Diabète type 2 |
|---|---|---|
| Effet incrétine total | 50-70 % | 20-30 % |
| Réponse au GIP | Normale | Severement réduite |
| Réponse au GLP-1 | Normale | Partiellement preservee |
| Sécrétion de GLP-1 | Normale | Légèrement réduite |
| Sécrétion de GIP | Normale | Normale ou augmentee |
Source : Nauck MA, Meier JJ. Diabetologia. 2011;54(1):10-18.
Ce paradoxe a ete resolu par la decouverte que l’activation pharmacologique supraphysiologique du récepteur GIP (comme celle produite par le tirzépatide) peut restaurer la sensibilite au GIP chez les patients diabétiques, surpassant même la réponse physiologique normale.
Synergie GLP-1 + GIP : pourquoi 1 + 1 = 3
L’association des deux hormones produit des effets synergiques qui depassent la simple addition de leurs actions individuelles :
1. Sur la perte de poids : Le GLP-1 réduit l’appétit via le tronc cerebral et ralentit la vidange gastrique. Le GIP active des voies complémentaires dans l’hypothalamus et agit directement sur le tissu adipeux. Résultat : la perte de poids sous tirzépatide (22,5 %) est supérieure de 5 a 6 points de pourcentage a celle sous sémaglutide (16,9 %).
2. Sur le contrôle glycemique : La double stimulation insulino-secretoire potentialise la réponse pancreatique. La réduction de l’HbA1c est de 2,07 % sous tirzépatide 15 mg, contre 1,86 % sous sémaglutide 2 mg.
3. Sur la composition corporelle : Le GIP favorise la perte de masse grasse tout en preservant la masse maigre. L’étude SURMOUNT-1 a montre que 85 % de la perte de poids provenait de la masse grasse sous tirzépatide, un ratio supérieur a celui observe sous sémaglutide.
4. Sur la tolérance : Le biais de signalisation du tirzépatide sur le récepteur GLP-1 (favorisant la voie AMPc par rapport à la beta-arrestine) réduit les effets gastro-intestinaux. Les nausées sont généralement moins sévères et de plus courte durée que sous sémaglutide.
Applications thérapeutiques actuelles et futures
La comprehension de la physiologie des incrétines a permis le développement de quatre classes de médicaments :
- Inhibiteurs de la DPP-4 (sitagliptine, vildagliptine) : empechent la degradation des incrétines naturelles. Effets modestes sur le poids et la glycémie.
- Agonistes du récepteur GLP-1 (sémaglutide, liraglutide, dulaglutide) : miment l’action du GLP-1 avec une durée d’action prolongee.
- Double agoniste GIP/GLP-1 (tirzépatide) : première molecule a activer les deux récepteurs simultanement.
- Triple agoniste GIP/GLP-1/glucagon (retatrutide, en phase 3) : ajoute le récepteur du glucagon pour augmenter encore la dépense énergétique.
Ce qu’il faut retenir
Le GLP-1 et le GIP sont deux hormones complémentaires qui, ensemble, controlent plus de la moitie de la réponse insulinique après un repas. Tandis que le GLP-1 agit principalement sur l’appétit, la vidange gastrique et le système cardiovasculaire, le GIP joue un rôle unique dans le métabolisme du tissu adipeux et la formation osseuse. Le tirzépatide exploite cette complementarite pour produire des résultats cliniques supérieurs aux traitements ciblant une seule hormone.
FAQ
Quelle est la différence entre GLP-1 et GIP ?
Le GLP-1 agit principalement sur l’appétit (via le cerveau), la vidange gastrique et le pancreas. Le GIP cible davantage le tissu adipeux, le métabolisme osseux et la réponse insulinique pancreatique. Les deux sont des hormones incrétines secretees par l’intestin après un repas.
Pourquoi le GIP a-t-il ete longtemps ignore dans les traitements ?
Chez les patients diabétiques, la réponse naturelle au GIP est très alteree. Les chercheurs pensaient donc que cibler le GIP serait inefficace. Le tirzépatide a prouve le contraire : l’activation pharmacologique à des doses supraphysiologiques restaure et amplifie les effets du GIP.
Le GLP-1 naturel dure-t-il longtemps dans le corps ?
Non. Le GLP-1 naturel à une demi-vie de seulement 2 a 3 minutes avant d’être degrade par l’enzyme DPP-4. C’est pourquoi les médicaments agonistes GLP-1 sont modifies chimiquement pour resister a cette degradation et durer plusieurs jours.
Le tirzépatide stimule-t-il les deux hormones ou les remplace-t-il ?
Le tirzépatide ne stimule pas la sécrétion naturelle de GLP-1 et GIP. Il remplace leur action en activant directement leurs récepteurs cellulaires, comme une clé qui ouvrirait deux serrures différentes simultanement.
Les inhibiteurs de la DPP-4 sont-ils aussi efficaces que les agonistes ?
Non. Les inhibiteurs de la DPP-4 (comme la sitagliptine) empechent la degradation des incrétines naturelles mais n’augmentent leurs niveaux que de 2 a 3 fois. Les agonistes comme le tirzépatide atteignent des concentrations 10 a 100 fois supérieures aux niveaux physiologiques, produisant des effets bien plus puissants sur le poids et la glycémie.
Sources
- Nauck MA, Meier JJ. The incretin effect in healthy individuals and those with type 2 diabetes. Diabetologia. 2011;54(1):10-18.
- Muller TD et al. GIP and GLP-1 as therapeutic targets in diabetes and obesity. Nat Rev Drug Discov. 2022;21:513-532.
- Turton MD et al. A rôle for glucagon-like peptide-1 in the central régulation of feeding. Nature. 1996;379:69-72.
- Kaneko K et al. GIP receptor signaling in neurons mediates body weight réduction. Cell Metabolism. 2023.
- Campbell JE, Drucker DJ. Pharmacology, physiology, and mechanisms of incretin hormone action. Cell Metab. 2013;17(6):819-837.
- Holst JJ. The physiology of glucagon-like peptide 1. Physiol Rev. 2007;87(4):1409-1439.