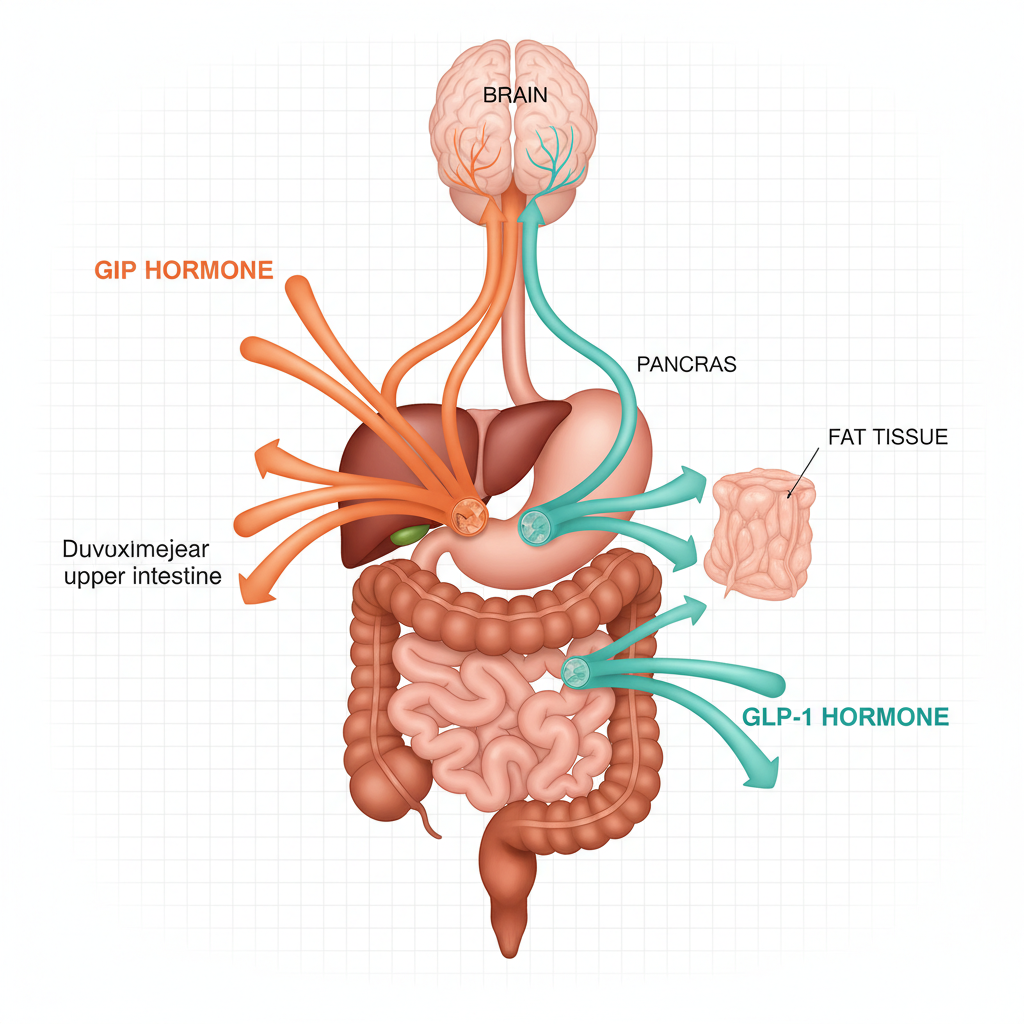
Os hormônios incretínicos GLP-1 e GIP desempenham um papel central na regulação do apetite, do metabolismo da glicose e do peso corporal. Compreender seu funcionamento permite entender melhor por que o tirzepatida (Mounjaro), que visa esses dois hormônios simultaneamente, obtém resultados superiores aos tratamentos monoagonistas.
Incretinas: hormônios digestivos essenciais
O conceito de incretina nasceu de uma observação clínica importante: a administração oral de glicose provoca uma secreção de insulina significativamente superior à obtida por injeção intravenosa da mesma quantidade de glicose. Este efeito incretina, descoberto na década de 1960, representa 50 a 70% da resposta insulínica pós-prandial total.
Dois hormônios são responsáveis por este efeito: o GLP-1 (peptídeo-1 semelhante ao glucagon) e o GIP (polipeptídeo insulinotrópico dependente de glicose). Secretados por células especializadas do intestino em resposta à ingestão de alimentos, eles orquestram uma cascata de sinais metabólicos que vão muito além da simples regulação da glicemia.
GLP-1: o hormônio da saciedade
O GLP-1 é sintetizado pelas células L do íleo distal e do cólon a partir do proglucagon, um precursor peptídico. Sua secreção começa 10 a 15 minutos após o início de uma refeição, com um pico atingido entre 30 e 60 minutos.
Mecanismos de ação do GLP-1:
No pâncreas: O GLP-1 liga-se ao seu receptor (GLP-1R) nas células beta pancreáticas, estimulando a secreção de insulina de forma glicose-dependente. Isso significa que o efeito insulino-secretor só se manifesta quando a glicemia está elevada, o que minimiza o risco de hipoglicemia. Ele também inibe a secreção de glucagon pelas células alfa, reduzindo a produção hepática de glicose.
No cérebro: Os receptores de GLP-1 estão presentes em várias regiões cerebrais envolvidas no controle do apetite: o núcleo do trato solitário (NTS) no tronco cerebral, o núcleo arqueado do hipotálamo e a área postrema. A ativação desses receptores reduz os sinais de fome e aumenta a sensação de saciedade. O GLP-1 também modula o sistema de recompensa dopaminérgico, diminuindo o desejo por alimentos ricos em gorduras e açúcares (Turton et al., Nature, 1996).
No estômago: O GLP-1 retarda significativamente o esvaziamento gástrico, o que prolonga a distensão do estômago e os sinais mecânicos de saciedade. Este efeito explica em parte as náuseas observadas no início do tratamento com agonistas de GLP-1.
No sistema cardiovascular: Receptores de GLP-1 são expressos em cardiomiócitos e células endoteliais. O GLP-1 melhora a função endotelial, reduz a inflamação vascular e possui efeitos cardioprotetores demonstrados em grandes estudos cardiovasculares (LEADER, SUSTAIN-6, SELECT).
Meia-vida natural do GLP-1: apenas 2 a 3 minutos. A enzima DPP-4 (dipeptidil peptidase-4) degrada rapidamente o GLP-1 em metabólitos inativos. Foi essa degradação ultrarrápida que exigiu o desenvolvimento de formas resistentes (análogos de GLP-1) ou de inibidores da DPP-4.
GIP: o hormônio metabólico subestimado
O GIP é secretado pelas células K do duodeno e jejuno proximal. Sua secreção é desencadeada principalmente pela absorção de glicose e lipídios, com um pico plasmático atingido 15 a 30 minutos após a refeição.
Por muito tempo considerado um hormônio menor na fisiologia metabólica, o GIP tem sido objeto de uma reavaliação completa desde os trabalhos de Muller et al. (Nature Reviews Drug Discovery, 2022).
Mecanismos de ação do GIP:
No pâncreas: O GIP é o mais potente estimulador da secreção de insulina entre as incretinas, responsável por aproximadamente 60% do efeito incretina total. Assim como o GLP-1, sua ação é glicose-dependente. Ele também estimula a proliferação e a sobrevivência das células beta pancreáticas.
No tecido adiposo: É aqui que o GIP se distingue fundamentalmente do GLP-1. Os receptores de GIP (GIP-R) são fortemente expressos no tecido adiposo branco. A ativação do GIP-R no tecido adiposo produz efeitos complexos e dependentes do contexto:
- Em condições fisiológicas normais: o GIP favorece o armazenamento de lipídios e a adipogênese
- Em ativação farmacológica sustentada (como com o tirzepatida): ele favorece a lipólise, a mobilização de gorduras e o escurecimento do tecido adiposo branco
- Ele melhora a sensibilidade à insulina no tecido adiposo
- Ele reduz a inflamação adipocitária crônica associada à obesidade
No cérebro: Receptores de GIP estão presentes no hipotálamo, córtex cerebral e hipocampo. O GIP modula o apetite por vias distintas das do GLP-1, atuando notadamente na motivação alimentar e nos circuitos de recompensa. Estudos em camundongos mostram que a ativação de neurônios GIP-R no hipotálamo reduz a ingestão alimentar de forma independente do GLP-1 (Kaneko et al., Cell Metabolism, 2023).
Nos ossos: O GIP estimula a formação óssea ativando os osteoblastos e inibindo parcialmente a reabsorção óssea. É por isso que o tirzepatida pode ter uma vantagem sobre os agonistas puros de GLP-1 para a preservação da densidade óssea durante a perda de peso.
Meia-vida natural do GIP: aproximadamente 5 a 7 minutos, também degradado pela DPP-4.
A diferença entre pacientes saudáveis e diabéticos
Um paradoxo há muito tempo dificultou o desenvolvimento de terapias baseadas no GIP: em pacientes com diabetes tipo 2, a resposta insulínica ao GIP é severamente alterada. O efeito incretina é reduzido em 80% em comparação com indivíduos saudáveis.
| Parâmetro | Indivíduo saudável | Diabetes tipo 2 |
|---|---|---|
| Efeito incretina total | 50-70 % | 20-30 % |
| Resposta ao GIP | Normal | Severamente reduzida |
| Resposta ao GLP-1 | Normal | Parcialmente preservada |
| Secreção de GLP-1 | Normal | Levemente reduzida |
| Secreção de GIP | Normal | Normal ou aumentada |
Fonte: Nauck MA, Meier JJ. Diabetologia. 2011;54(1):10-18.
Este paradoxo foi resolvido pela descoberta de que a ativação farmacológica suprafisiológica do receptor de GIP (como a produzida pelo tirzepatida) pode restaurar a sensibilidade ao GIP em pacientes diabéticos, superando até mesmo a resposta fisiológica normal.
Sinergia GLP-1 + GIP: por que 1 + 1 = 3
A associação dos dois hormônios produz efeitos sinérgicos que superam a simples adição de suas ações individuais:
1. Na perda de peso: O GLP-1 reduz o apetite via tronco cerebral e retarda o esvaziamento gástrico. O GIP ativa vias complementares no hipotálamo e atua diretamente no tecido adiposo. Resultado: a perda de peso com tirzepatida (22,5%) é 5 a 6 pontos percentuais superior à obtida com semaglutida (16,9%).
2. No controle glicêmico: A dupla estimulação insulino-secretora potencializa a resposta pancreática. A redução da HbA1c é de 2,07% com tirzepatida 15 mg, contra 1,86% com semaglutida 2 mg.
3. Na composição corporal: O GIP favorece a perda de massa gorda enquanto preserva a massa magra. O estudo SURMOUNT-1 mostrou que 85% da perda de peso com tirzepatida veio da massa gorda, uma proporção superior à observada com semaglutida.
4. Na tolerabilidade: O viés de sinalização do tirzepatida no receptor de GLP-1 (favorecendo a via AMPc em relação à beta-arrestina) reduz os efeitos gastrointestinais. As náuseas são geralmente menos graves e de menor duração do que com semaglutida.
Aplicações terapêuticas atuais e futuras
A compreensão da fisiologia das incretinas permitiu o desenvolvimento de quatro classes de medicamentos:
- Inibidores da DPP-4 (sitagliptina, vildagliptina): impedem a degradação das incretinas naturais. Efeitos modestos no peso e na glicemia.
- Agonistas do receptor de GLP-1 (semaglutida, liraglutida, dulaglutida): mimetizam a ação do GLP-1 com duração de ação prolongada.
- Agonista duplo GIP/GLP-1 (tirzepatida): primeira molécula a ativar ambos os receptores simultaneamente.
- Agonista triplo GIP/GLP-1/glucagon (retatrutida, em fase 3): adiciona o receptor de glucagon para aumentar ainda mais o gasto energético.
O que reter
O GLP-1 e o GIP são dois hormônios complementares que, juntos, controlam mais da metade da resposta insulínica após uma refeição. Enquanto o GLP-1 atua principalmente no apetite, no esvaziamento gástrico e no sistema cardiovascular, o GIP desempenha um papel único no metabolismo do tecido adiposo e na formação óssea. O tirzepatida explora essa complementaridade para produzir resultados clínicos superiores aos tratamentos que visam apenas um hormônio.
FAQ
Qual a diferença entre GLP-1 e GIP?
O GLP-1 atua principalmente no apetite (via cérebro), esvaziamento gástrico e pâncreas. O GIP visa mais o tecido adiposo, o metabolismo ósseo e a resposta insulínica pancreática. Ambos são hormônios incretínicos secretados pelo intestino após uma refeição.
Por que o GIP foi ignorado por tanto tempo nos tratamentos?
Em pacientes diabéticos, a resposta natural ao GIP é muito alterada. Os pesquisadores pensavam, portanto, que visar o GIP seria ineficaz. O tirzepatida provou o contrário: a ativação farmacológica em doses suprafisiológicas restaura e amplifica os efeitos do GIP.
O GLP-1 natural dura muito tempo no corpo?
Não. O GLP-1 natural tem uma meia-vida de apenas 2 a 3 minutos antes de ser degradado pela enzima DPP-4. É por isso que os medicamentos agonistas de GLP-1 são quimicamente modificados para resistir a essa degradação e durar vários dias.
O tirzepatida estimula os dois hormônios ou os substitui?
O tirzepatida não estimula a secreção natural de GLP-1 e GIP. Ele substitui a ação deles ativando diretamente seus receptores celulares, como uma chave que abriria duas fechaduras diferentes simultaneamente.
Os inibidores da DPP-4 são tão eficazes quanto os agonistas?
Não. Os inibidores da DPP-4 (como a sitagliptina) impedem a degradação das incretinas naturais, mas aumentam seus níveis apenas 2 a 3 vezes. Agonistas como o tirzepatida atingem concentrações 10 a 100 vezes superiores aos níveis fisiológicos, produzindo efeitos muito mais potentes no peso e na glicemia.
Fontes
- Nauck MA, Meier JJ. The incretin effect in healthy individuals and those with type 2 diabetes. Diabetologia. 2011;54(1):10-18.
- Muller TD et al. GIP and GLP-1 as therapeutic targets in diabetes and obesity. Nat Rev Drug Discov. 2022;21:513-532.
- Turton MD et al. A rôle for glucagon-like peptide-1 in the central régulation of feeding. Nature. 1996;379:69-72.
- Kaneko K et al. GIP receptor signaling in neurons mediates body weight réduction. Cell Metabolism. 2023.
- Campbell JE, Drucker DJ. Pharmacology, physiology, and mechanisms of incretin hormone action. Cell Metab. 2013;17(6):819-837.
- Holst JJ. The physiology of glucagon-like peptide 1. Physiol Rev. 2007;87(4):1409-1439.